
近日,天使母基金合作子基金投資項(xiàng)目士澤生物醫(yī)藥(蘇州)有限公司(Roche Accelerator Member;姑蘇重大創(chuàng)新團(tuán)隊(duì);以下簡稱“士澤生物”)聯(lián)合上海市東方醫(yī)院(同濟(jì)大學(xué)附屬東方醫(yī)院)劉中民團(tuán)隊(duì)等順利完成 “臨床級iPSC衍生亞型神經(jīng)前體細(xì)胞治療漸凍癥(肌萎縮側(cè)索硬化癥;ALS)”的全球首例患者入組。
此前,經(jīng)過多輪嚴(yán)格評審,本項(xiàng)臨床研究正式由國家兩委局批準(zhǔn),作為國家級干細(xì)胞備案臨床研究項(xiàng)目正式開展:本臨床研究項(xiàng)目是我國首個(gè)及迄今唯一正式獲批開展的iPSC衍生細(xì)胞藥治療漸凍癥的臨床研究,也是全球首例/首個(gè)異體通用型臨床級iPSC衍生神經(jīng)細(xì)胞再生治療漸凍癥的臨床研究。正式獲批開展的本國家級臨床研究項(xiàng)目正依據(jù)我國CDE發(fā)布的《人源性干細(xì)胞產(chǎn)品藥學(xué)研究與評價(jià)技術(shù)指導(dǎo)原則》及 《人源性干細(xì)胞及其衍生細(xì)胞治療產(chǎn)品臨床試驗(yàn)技術(shù)指導(dǎo)原則》等指南文件,根據(jù)《干細(xì)胞臨床研究管理辦法(試行)》(國衛(wèi)科教發(fā)〔2015〕48號(hào))和《干細(xì)胞制劑質(zhì)量控制和臨床前研究指導(dǎo)原則(試行)》(國衛(wèi)辦科教發(fā)〔2015〕46號(hào))等指導(dǎo)原則規(guī)范開展。

此次士澤生物正式由國家兩委局獲批開展的臨床研究,采用士澤生物自主開發(fā)的用于治療漸凍癥的臨床級iPSC衍生亞型神經(jīng)前體細(xì)胞新藥(FIC),該全球創(chuàng)新性產(chǎn)品已于2023年獲得美國食品藥品監(jiān)督管理局(FDA)認(rèn)證授予全球孤兒藥(Orphan Drug Designation,ODD)資格:為首個(gè)中國自主iPSC衍生細(xì)胞藥獲得FDA認(rèn)證并授予孤兒藥資格、也是迄今為止全球首個(gè)用于治療漸凍癥的擁有孤兒藥資格的iPSC衍生細(xì)胞藥物(【全球首發(fā)】士澤生物國產(chǎn)iPSC衍生細(xì)胞藥獲FDA認(rèn)證授予孤兒藥資格!)。
“漸凍癥”(肌萎縮側(cè)索硬化癥;ALS)是一種運(yùn)動(dòng)神經(jīng)元病及進(jìn)行性神經(jīng)退行性疾病,漸凍癥患者俗稱漸凍人。漸凍癥患者的運(yùn)動(dòng)神經(jīng)元持續(xù)退行性病變和死亡,導(dǎo)致患者出現(xiàn)上、下運(yùn)動(dòng)神經(jīng)元合并受損,最終可導(dǎo)致癱瘓,從無法行走到無法說話、吞咽、呼吸。臨床數(shù)據(jù)顯示,漸凍癥患者的平均存活期約39個(gè)月,目前尚無能夠?qū)嵸|(zhì)性緩解或挽救漸凍癥的有效臨床藥物及臨床解決方案。因此,迫切需要開發(fā)新的治療方案。
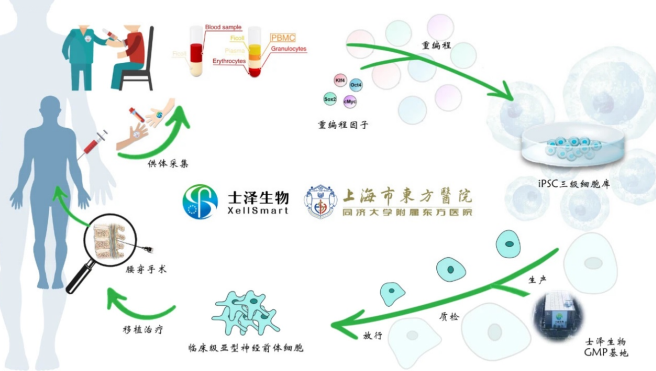
此次士澤生物聯(lián)合合作醫(yī)院獲國家兩委局正式批準(zhǔn)開展的國家級干細(xì)胞備案臨床研究項(xiàng)目,依托士澤生物已建立完成的>5000平方米的研發(fā)中心、GMP中試基地及質(zhì)控中心,可充分保障本次獲批的國家級臨床研究項(xiàng)目開展所需的臨床級iPSC衍生亞型神經(jīng)前體細(xì)胞制劑的生產(chǎn)、質(zhì)控和放行。此次士澤生物獲批的國家級干細(xì)胞臨床研究備案項(xiàng)目,采用腰穿注射方式移植士澤生物異體通用型臨床級iPSC衍生亞型神經(jīng)前體細(xì)胞全球孤兒藥,用于移植治療漸凍癥:對研究再生神經(jīng)細(xì)胞移植治療漸凍癥的安全性并分析對漸凍癥患者療效的影響具有重要的全球首創(chuàng)式臨床意義。
迄今為止,士澤生物已獲得由國家兩委局正式批準(zhǔn)開展的全部兩項(xiàng)iPSC衍生細(xì)胞治療神經(jīng)系統(tǒng)疾病的國家級備案臨床研究項(xiàng)目,用于治療中重度帕金森病及漸凍癥。在士澤生物已開展的另一項(xiàng)國家級備案臨床研究中:士澤生物已與合作醫(yī)院完成多例經(jīng)紋狀體雙側(cè)殼核立體定位注射移植臨床級iPSC衍生中腦多巴胺能神經(jīng)前體細(xì)胞,用于治療中重度帕金森病患者,其中包括在中國上海完成的中國首例臨床級iPSC衍生多巴胺能神經(jīng)前體細(xì)胞移植治療帕金森病。
迄今為止,士澤生物臨床級iPSC衍生細(xì)胞治療中重度帕金森病最長隨訪期已超過9個(gè)月以上,迄今無細(xì)胞療法相關(guān)不良事件出現(xiàn),且多例患者開關(guān)期時(shí)間及MDS-UPDRS評分量表等關(guān)鍵療效指標(biāo)及多項(xiàng)非運(yùn)動(dòng)指標(biāo)均有顯著性改善趨勢。士澤生物已開展的人體臨床研究的積極結(jié)果,為后續(xù)進(jìn)一步開展臨床試驗(yàn)提供了重要的鋪墊和關(guān)鍵的驗(yàn)證,該在研臨床項(xiàng)目已于近日順利通過國家衛(wèi)健委及現(xiàn)場核查專家組的臨床規(guī)范及GMP生產(chǎn)現(xiàn)場核查。
士澤生物iPSC衍生細(xì)胞治療帕金森病臨床受試者招募
受試者入組標(biāo)準(zhǔn):
1. 自愿參加本試驗(yàn),簽署知情同意書。并承諾遵守研究程序,配合實(shí)施全過程;
2. 30~70歲的原發(fā)性帕金森病患者,男女不限,病史5年以上;3.要求對左旋多巴反應(yīng)良好,LCT,最大改善率大于30%。
排除標(biāo)準(zhǔn):(符合以下任一條標(biāo)準(zhǔn)的對象將排除于本研究)
1. 非典型的帕金森病患者或繼發(fā)性帕金森綜合癥;
2. 嚴(yán)重的精神癥狀或癡呆;
3.有惡性腫瘤史,有癲癇發(fā)作史或預(yù)防性應(yīng)用抗癲癇藥,有睡眠呼吸暫停、慢性阻塞性肺、傳染病,凝血/肝功異常等;
4.MRI和PET禁忌病患者;
5.伴有重度異動(dòng)癥。
您將獲得交通補(bǔ)貼和營養(yǎng)費(fèi)。
咨詢方式:臨床研究聯(lián)絡(luò)人:13916342994(云老師)、18217048235(培老師)15850048704(包老師)
士澤生物iPSC衍生細(xì)胞治療漸凍癥臨床受試者招募
受試者入組標(biāo)準(zhǔn):
1.根據(jù)修訂的EL Escorial標(biāo)準(zhǔn)診斷明確或可能的ALS,篩選時(shí)距初次確診的時(shí)間為6~24個(gè)月之間;
2.年齡為18~60歲(包含界值),男女不限;
3.患者既往接受過標(biāo)準(zhǔn)治療后療效不佳或疾病進(jìn)展;
4.用力呼氣肺活量(FVC)≥70%;
5.男性患者及其配偶和育齡期女性患者應(yīng)同意從簽署ICF開始直至用藥后1年內(nèi)采取有效的避孕措施
6.患者具有良好的依從性。
受試者排除標(biāo)準(zhǔn):(符合以下任一條標(biāo)準(zhǔn)的對象將排除于本研究)
1.患有嚴(yán)重系統(tǒng)性疾病、自身免疫性疾病、惡性腫瘤或既往有惡性腫瘤史,以及任何其他可能危及患者或干擾研究結(jié)果解釋的疾病。
2.患有引起顱內(nèi)高壓的腦器質(zhì)性病變者;
3.被診斷為嚴(yán)重認(rèn)知障礙、臨床癡呆或重大精神疾病;
4.患者有全身炎癥或活動(dòng)性感染
5.既往接受過任何同種異體細(xì)胞治療或組織移植治療;
6.篩選期前三個(gè)月內(nèi)參加過其他臨床研究;
7.經(jīng)研究者判斷,患有其他控制不佳的全身性疾病,或不適合參加本項(xiàng)臨床研究的其它情況者
您將獲得交通補(bǔ)貼和營養(yǎng)費(fèi)。
咨詢方式:臨床研究聯(lián)絡(luò)人:13916342994(云老師)、18217048235(培老師)15850048704(包老師)
關(guān)于士澤生物
士澤生物由創(chuàng)始人李翔博士歸國全職創(chuàng)立,士澤生物專注于開發(fā)臨床級iPSC衍生細(xì)胞藥治療帕金森病等尚無實(shí)質(zhì)臨床解決方案的神經(jīng)系統(tǒng)疾病(核心主營業(yè)務(wù)):士澤生物組建了具有國際競爭力及產(chǎn)業(yè)界背景的全職團(tuán)隊(duì),建立了一批具有自主知識(shí)產(chǎn)權(quán)、國際領(lǐng)先的新技術(shù)、新平臺(tái),圍繞核心主營業(yè)務(wù)可持續(xù)自研創(chuàng)新。士澤生物已自主建設(shè)及運(yùn)營>5000平方米的研發(fā)中心、B+A級GMP基地及質(zhì)控中心的完整軟硬件平臺(tái),士澤生物自主開發(fā)的多項(xiàng)臨床級iPSC衍生細(xì)胞藥的研發(fā)管線已完成核心CMC開發(fā)、建立了全流程的臨床級制備工藝及質(zhì)量控制體系,并完成多種GMP級iPSC衍生亞型特化神經(jīng)前體細(xì)胞治療產(chǎn)品的正式注冊批及臨床批生產(chǎn)。
士澤生物擁有兩項(xiàng)臨床階段的iPSC衍生神經(jīng)細(xì)胞治療新藥,正在開展臨床級iPSC衍生神經(jīng)前體細(xì)胞治療中重度帕金森病及漸凍癥的兩項(xiàng)國家級備案干細(xì)胞臨床研究(均為中國首例/首個(gè)或全球首例/首個(gè)),擁有1項(xiàng)美國FDA全球孤兒藥認(rèn)定(為中國首個(gè)自主iPSC衍生細(xì)胞藥獲得FDA認(rèn)證并授予全球孤兒藥資格)。
士澤生物獲評姑蘇重大創(chuàng)新團(tuán)隊(duì)企業(yè)、江蘇省雙創(chuàng)領(lǐng)軍人才企業(yè)、姑蘇創(chuàng)新創(chuàng)業(yè)領(lǐng)軍人才企業(yè)等;連續(xù)獲評中國潛在獨(dú)角獸企業(yè)及江蘇省潛在獨(dú)角獸企業(yè);連續(xù)兩年獲得國家科技部全國顛覆性技術(shù)創(chuàng)新大賽優(yōu)勝獎(jiǎng)(最高獎(jiǎng))等。近2年內(nèi)士澤生物已完成逾三億元A輪/A+輪/B1輪市場化融資:由峰瑞資本、啟明創(chuàng)投、禮來亞洲基金、紅杉中國、金圓展鴻、中新資本、泰瓏/泰鯤資本等多家知名市場化機(jī)構(gòu)領(lǐng)投及共同投資。